Dobrý den,
moc vás prosím, mohl by mi někdo vysvětlit jak postupovat při počítání podtržených příkladů?
Děkuji.
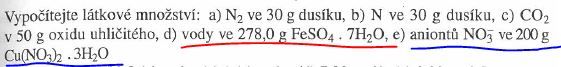
0x
Je to vcelku jednoduché, použiješ vzorec n = m/M, jen v některých případech musíš trochu uvažovat. Pokud bys potřeboval/-la vysvětlení, pošli mi svoji mailovou adresu, nebo mně kontaktuj na ICQ (463972984)
a: M(N2) = 28g/mol; n(N2) = 30/28 = 1,071molu; b: M(N) = 14g/mol; n(N) = 30/14 = 2,143 molu
c: M(CO2) = 44g/mol; n(CO2) = 50/44 = 1,136 molu;
d: M(FeSO4.7H2O) = 278g/mol; n(heptahydr.) = 278/278 = 1 mol; molekula heoptahydrátu obsahuje 7 molekul vody, takže:
n(H2O) = 7*n(heptahydr.) = 7molů.
e: M(Cu(NO3)2.3H2O) = 241,6g/mol; n(trihydr.) = 200/241,6 = 0,828molu; n(NO3-) = 2*n(trihydr.) = 2*0,828 = 1,656molu NO3-
OK?
0x
Tady je část článku, který jsem našel:
--Každý z nás se v úvodu studia chemie učil v nějaké podobě zákon stálých poměrů slučovacích, který pro každý chemický pochod vyjadřuje vyčíslená chemická rovnice: 2H2 + O2 = 2H2O -> dvě molekuly vodíku reagují s jednou molekulou kyslíku za vzniku dvou molekul vody. Jako každou rovnici, můžeme i vyčíslenou chemickou rovnici rozšířit tím, že všechny členy násobíme stejným číslem, na př. 4: 8H2 + 4O2 = 8H2O. Vzhledem k tomu, že obvyklá množství látek se skládají z velkého počtu molekul, používáme nejčastěji k takovému rozšíření Avogadrovu konstantu NA = 6,022*10na23. Tak z jedné molekuly dostaneme technicky přijatelnější jednotku - 1 mol. Mol nějakých částic je 6,022*10^23 těchto částic. Mol je číslo, podobně jako 4 nebo 256 a samo o sobě nemá smysl. Pokud má vyjadřovat počet částic, musí být doplněno údajem o druhu částic: 1 mol H2, 3 moly N2, 5 molů NH3, 0,5mol O (0,5 molů atomu kyslíku).
--Příklad amoniaku nám poslouží k podrobnějšímu pohledu: 5 molů NH3 obsahuje tedy 5*6,022*10^23 molekul NH3. Každá z těchto molekul obsahuje 1 atom N a 3 atomy vodíku. 5 molů NH3 tedy obsahuje 5 molů atomů N a 3*5 = 15 molů atomů H. Podobně 1 mol H2 (molekulárního vodíku) obsahuje 2*1 mol H (atomů vodíku, atomárního vodíku). Veličinu, která vyjadřuje množství látky tímto způsobem, nazýváme "látkové množství" a značíme ji "n". Na příklad n(CO2) = 5mol. V našem příkladu s amoniakem bychom tedy mohli napsat: n(NH3) = n(N) = n(H)/3 => n(H) = 3*n(N) = 3*n(NH3) tedy mol amoniaku obsahuje 3 moly atomů vodíku. Nebo složitější příklad: Na2SO4: n(Na2SO4) = n(Na)/2 = n(S) = n(O)/4 => n(O) = 4*n(Na2SO4) látkové množství atomů kyslíku v síranu sodném je čtyřnásobkem látkového množství síranu sodného.
- Výpočty látkové množství
- Výpočty molární hmotnost látkové množ
- Fyzika-kruhovy dej s id. plynem-přiklady
- Chemické výpočty-9.ročník
- Molární hmonost, látkové množství
- Přiklad - titrace
- Kys. sírová výpočet
- Úloha z chemie
- Látkové množství plynu
- Hmotnost a množství
- Faradayovy zákony
- Výpočet hmotnosti roztoku
- Hmotnostní zlomek
- Chemie přiklady srážecí titrace
- Výpočet titrace do chemie
Neneseme odpovědnost za správnost informací a za škodu vzniklou jejich využitím. Jednotlivé odpovědi vyjadřují názory jejich autorů a nemusí se shodovat s názorem provozovatele poradny Poradte.cz.
Používáním poradny vyjadřujete souhlas s personifikovanou reklamou, která pomáhá financovat tento server, děkujeme.