Nejste přihlášen/a.
Ahoj,
v chemii se učíme o elektronové konfiguraci a mně není nějak jasná. Jak ji zjistím, když mi někdo řekne, udělej elek. konfiguraci např. Li. Dá se to zjistit z hlavy? Nebo potřebuji tabulky. Znám hlavní kvantové číslo, to je 1 až nevím kolik. Dále vedlejší kvantové číslo s, p, d, f a magnetické, to jsou ty šipky. Pro názornost přikládám fotku. Díky moc.
2x
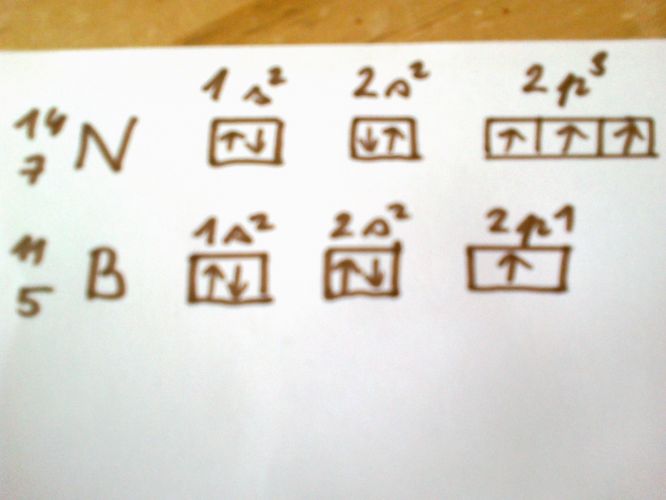
No, uděláš si ty rámečky (viz níže) a pak je vyplňuješ spinovýma šipkama. Šipek umístíš tolik, kolik má elektricky vyvážený atom protonů, v prvním případě tedy celkem sedm, ve druhém pět. Při vyplňování postupuješ tak, že v každé skupině okýnek nejdřív dáš všechny šipky jedním směrem a pak doplňuješ směr opačný. Takže s číslem 7: jednu nahoru, víc nejde, jednu dolů. Druhou skupinu okýnek (skupinu - je tam zas jen jedno) stejně. Třetí skupina, zbývají tři šipky, všechny tři se vejdou směrem nahoru. Kdybys měl číslo 6, budou dvě nahoru, kdybys měl 8, dáš tři nahoru a pak teprv tu úplně poslední dáš do prvního okýnka dolů. Je to jako v autobuse, lidi si nejdřív sedaj sami, až pak se tvořej dvojice.
A jak přijít na ty rámečky .. seřadí se to podle energetických hladin od nejmenší. K hlavnímu číslu se přiřazují čísla vedlejší, všechna, která se "vejdou", k 1 jedno písmeno, ke 2 dvě, ke 3 tři, ke 4 všechny. Takže 1s, 2s, 2p, 3s, 3p, 3d, 4s, 4p, 4d, 5s, 4f, 5p, 5d atd. Určitě sis všimnul, že mám 5s a 4f prohozené, je to kvůli těm energetickým hladinám, kdy 4f by už bylo víc než 5s, tak se dá 5s dřív a pak se doplní opomenutý 4f. Jestli to je ale přesně takhle si nejsem jistej, je to už spousta let, co jsme se to učili, měl bys radši konzultovat učebnici ![]() Každopádně existoval vzorec, kterým sis na základě čísla a písmena tu energii spočítal a pak porovnal, co přijde dřív. Rámečky pak mají počet okýnek podle písmena, s má jedno, p tři, d pět a f sedm.
Každopádně existoval vzorec, kterým sis na základě čísla a písmena tu energii spočítal a pak porovnal, co přijde dřív. Rámečky pak mají počet okýnek podle písmena, s má jedno, p tři, d pět a f sedm.
To je snad tak nějak všechno ..
Díky moc. Ty šipky jsem pochopila. Ale nemůžu přijít na to, jak zjistím, např. elekt. konfiguraci flouru. Vím, že má 19 nukleonů a 9 protonů. S toho vyplývá, že tam bude 9 šipek. A mám začít takhle? Viz. fotka. Takže jsem umístila čtyři elektrony, zbývá mi 5 elektronů, které nevím, jak mám umístit. Nevím, zda mám ten postup správně.
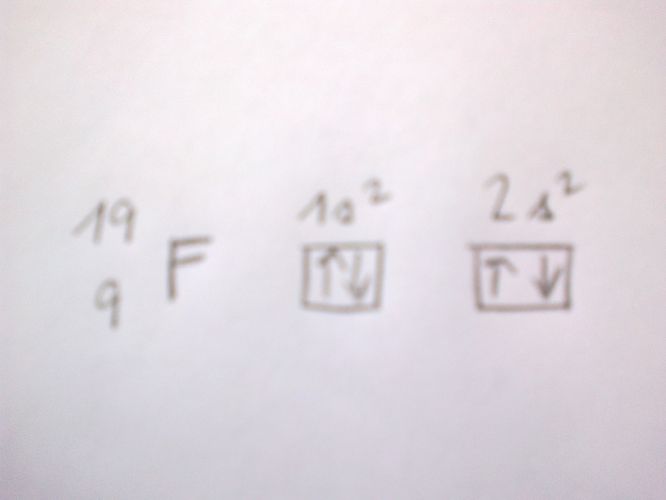
To jsem se snažil vysvětlit v druhém odstavci. Nakonec se to pořadí mění už u d, ne až u f, takže jsem to měl špatně.
Výstavbový princip (princip minimální energie):
Orbitaly s energií nižší se zaplňují dříve než orbitaly s energií vyšší, energie orbitalů se zvyšuje s rostoucí hodnotou součtu hlavního a vedlejšího kvantového čísla (n+l), v případě shody rozhoduje hodnota hlavního kvantového čísla.
Energie roste v pořadí: 1s 2s 2p 3s 3p 4s 3d 4p 5s 4d 5p 6s 4f 5d 6p 7s 5f 6d 7p
Nebude to takhle?
doplněno 17.09.11 12:56:Takže to chápu dobře, vyberu si ještě jeden prvek a zkusím to. Pak to sem hodím. Mohl bys mi to zkontrolovat? Děkuji moc. Bude to ale nejspíš až po obědě. ![]()
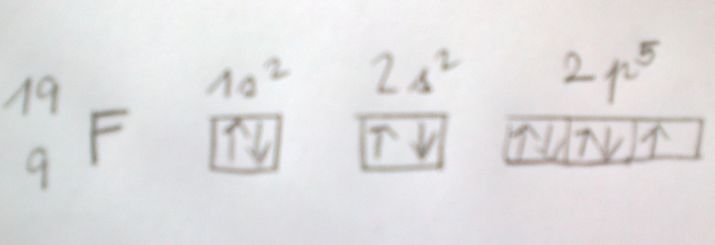
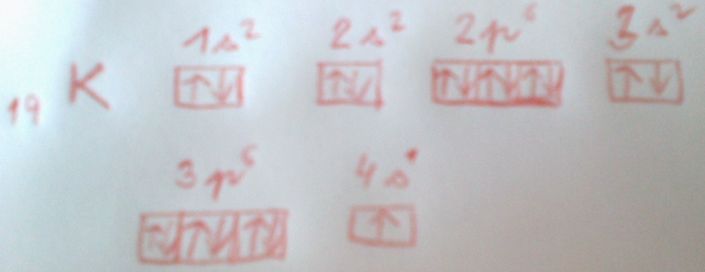
No právě zrovna ta měď a chrom, stříbro, zlato.. Zjednodušeně jde o to, že je lepší, když jsou orbitaly (ty chlívečky) zaplněné úplně nebo napůl (= všechny chlívečky jsou zaplněny šipkami jen jedním směrem), takže je pro Cr lepší, když má 3d5 4s1 než 3d4 4s2. Zkus se podívat sem, je to tam docela hezky vysvětleno - i to, jak jde po sobě 1s, 2s, 2p,... A jsou tam vyznačené i ty výjimky. fp.tul.cz/...
![]() V podstatě, jen 3d je před 4s: 1s22s22p63s23p63d54s1. Je to zase kvůli energiím. Jo a ještě jedna drobnost - máš tam napsané 3d4 místo 3d5, ale to je jen překlep, šipeček máš pět
V podstatě, jen 3d je před 4s: 1s22s22p63s23p63d54s1. Je to zase kvůli energiím. Jo a ještě jedna drobnost - máš tam napsané 3d4 místo 3d5, ale to je jen překlep, šipeček máš pět ![]() Teda jestli dobře vidím, je to rozmazané. Vždycky si to můžeš odkontrolovat tady: tabulka.cz/...
Teda jestli dobře vidím, je to rozmazané. Vždycky si to můžeš odkontrolovat tady: tabulka.cz/...
- Elektronová konfigurace
- Elektronová konfigurace - excitovaný stav
- Elektronová konfigurace
- Počet atomových orbitalů
- Kovalentní vazby a oxidační čísla
- Elektronová konfigutace
- Elektronová konfigurace, bez vystavového pri
- Elektronová konfigurace
- Proč je rtuť kapalná?
- Periodická tabulka prvků - elektronová konfigurace
- Kolik má sodík val. elekronů?
- Elektronová konfigurace
- Elektronová konfigurace d prvků
- Dusík a jeho slouceniny
- Elektronová konfigurace vanadu
Neneseme odpovědnost za správnost informací a za škodu vzniklou jejich využitím. Jednotlivé odpovědi vyjadřují názory jejich autorů a nemusí se shodovat s názorem provozovatele poradny Poradte.cz.
Používáním poradny vyjadřujete souhlas s personifikovanou reklamou, která pomáhá financovat tento server, děkujeme.