Nejste přihlášen/a.
0x
Mám pocit, že moje příspěvky nečteš, ani v jednom případě nebyla nějaká odezva. Ale ještě jednou zkusím:
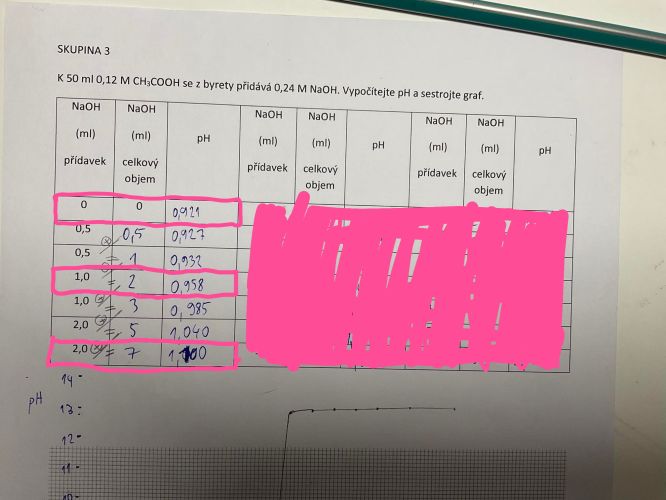
Nejprve si spočítáme nějaké údaje: n(CH3COOH) = 0,05dm3*0,12 = 0,006 mol; V 1 cm3 roztoku NasOH je
n(NaOH) = 0,001dm3*0,24 = 0,00024 mol NaOH.. A teď už budeme počítat:
1: jde o roztok slabé kyseliny o c = 0,12 mol/dm3; pH = 0,5*(pKa-log(ca)) = 0,5*(4,75-log(0,12)) = 2,83
Dál už budeme počítat pufry, protože přídavek NaOH sníží množství kyseliny a vytvoří stejné množství soli:
2: 2cm3 NaOH = 0,00048 mol NaOH, to bude látkové množství soli ns. Látkové množství kyseliny bude 0,006-0,00048 = 0,00552mol (na). poměr ns/na = 0,00048/0,00552 = 0,087; pH = pKa + log(ns/na) = 4,75 + log(0,087) = 3,69
3: Celkový přídavek je 7cm3. n(NaOH) = ns = 0,00024*7 = 0,00168mol; na = 0,006-0,00168 = 0,00432mol
ns/na = 0,00168/0,00432 = 0,389 => pH = 4,75 + log(0,389) = 4,34
Na závěr - dokud se bude jednat o pufr, nebude záležet na koncentraci a tedy ani na růstu objemu. Ten bude mít vliv až v bodu ekvivalence a za ním jako koncentrace nadbytečného NaOH. V bodě ekvivalence bude pH určovat koncentrace CH3COO-, jako konjugované slabé báze kyseliny octové s pKb = 14 - pKa = 9,25.
Nějaké nejasnosti?
- Výpočty látkové množství
- Látkové množství - příklad-jak vypočítat
- Výpočty molární hmotnost látkové množ
- Fyzika-kruhovy dej s id. plynem-přiklady
- Molární hmonost, látkové množství
- Chemické výpočty-9.ročník
- Úloha z chemie
- Kys. sírová výpočet
- Přiklad - titrace
- Látkové množství plynu
- Hmotnost a množství
- Chemie přiklady srážecí titrace
- Faradayovy zákony
- Hmotnostní zlomek
- Výpočet hmotnosti roztoku
Neneseme odpovědnost za správnost informací a za škodu vzniklou jejich využitím. Jednotlivé odpovědi vyjadřují názory jejich autorů a nemusí se shodovat s názorem provozovatele poradny Poradte.cz.
Používáním poradny vyjadřujete souhlas s personifikovanou reklamou, která pomáhá financovat tento server, děkujeme.