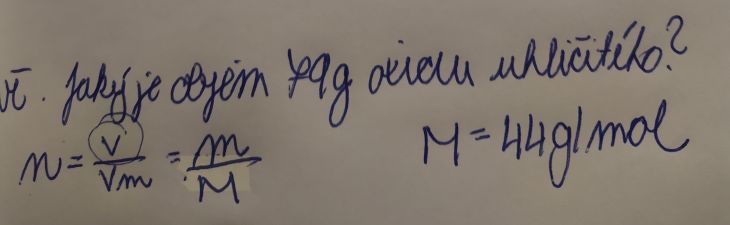Dobrý den, prosím jak by se řešil tento příklad? Vím že má vyjít asi 40 litrů.. ale nevím jak dojít k výsledku. Předem moc děkuji
1 odpověď na otázku
Řazeno dle hodnocení
0x
Máš tam vztah V/Vm = m/M. Ještě musíš vědět, že Vm je molární objem (= objem 1 molu ideálního plynu. Za "normálních podmínek - 101325Pa a 273,15K = 0°C ) je to 22,4 dm3/mol. Do vztahu na počátku dosadíš známe hodnoty a vypočítáš neznamou V:
V = Vm*m/M é= 22,4*79/44 = 40,22 dm3, samořejmě za dané teploty a tlaku.
OK?
Přihlásit se k odběru odpovědí z této otázky:
Otázky na téma látkové množství
- Výpočty látkové množství
- Látkové množství - příklad-jak vypočítat
- Výpočty molární hmotnost látkové množ
- Fyzika-kruhovy dej s id. plynem-přiklady
- Chemické výpočty-9.ročník
- Molární hmonost, látkové množství
- Přiklad - titrace
- Kys. sírová výpočet
- Úloha z chemie
- Látkové množství plynu
- Hmotnost a množství
- Faradayovy zákony
- Hmotnostní zlomek
- Výpočet hmotnosti roztoku
- Chemie přiklady srážecí titrace
Neneseme odpovědnost za správnost informací a za škodu vzniklou jejich využitím. Jednotlivé odpovědi vyjadřují názory jejich autorů a nemusí se shodovat s názorem provozovatele poradny Poradte.cz.
Používáním poradny vyjadřujete souhlas s personifikovanou reklamou, která pomáhá financovat tento server, děkujeme.